化学反応の背後にある力学を探求する中で、平衡定数 何を意味するかは非常に重要な概念です。この定数は反応物と生成物の濃度比を示し、私たちがどのように反応が進行するかを理解する手助けとなります。平衡定数は単なる数字以上のものであり、化学反応の動態や条件によって変わることがあります。
私たちはこのブログ記事を通じて、平衡定数 何を意味するかについて詳しく考察します。この重要な指標が科学研究や産業プロセスにおいてどれほど影響力があるか、その実用的な側面にも触れていきます。あなたはこの知識を持つことでどんな新しい視点が得られるでしょうか?ぜひ一緒に深掘りしていきましょう。
平衡定数 何を意味するのか
平衡定数は、化学反応が平衡状態に達したときの反応物と生成物の濃度比を示す重要な指標です。この値は、特定の条件下での反応の進行具合や方向性を理解する上で欠かせないものです。具体的には、平衡定数が大きい場合は生成物が主に存在し、小さい場合は反応物が優勢であることを示しています。このため、私たち化学者はこの値を用いて多くの化学プロセスや実験結果を解析します。
平衡定数とその表現
平衡定数は一般的に「K」と表されます。その計算式は以下の通りです:
[ K = frac{[C]^c[D]^d}{[A]^a[B]^b} ]
ここで、
- ( [A], [B], [C], [D] ) は、それぞれの成分のモル濃度
- ( a, b, c, d ) は、それぞれの成分に対する係数(化学反応式から抽出)
このようにして得られるK値によって、私たちはどちら側へのシフトが起こるか予測できます。
平衡状態との関連性
平衡状態とは、反応物と生成物間で相互作用が停止し、それぞれの濃度が一定になる状態を指します。この時点では、逆方向への反応速度と正方向への反応速度が等しくなります。これは、自発的な変化がなくなることを意味し、この時点で得られるK値は、その特定条件下でのみ有効です。
平衡定数について知識を深めることで、我々はより複雑な化学系についても理解できるようになります。また、この知識は実際的なアプリケーションにも役立つため、多岐にわたる産業や研究領域で重要視されています。
平衡定数の役割と重要性
平衡定数は、化学反応において非常に重要な役割を果たしています。この値は、特定の条件下での反応物と生成物の濃度比を示すだけでなく、反応がどの程度進行するかやその方向性を理解するためにも不可欠です。私たちがさまざまな化学プロセスを解析する際には、この平衡定数が指針となります。
平衡定数の重要性は以下の点に集約されます:
- 反応の予測:平衡定数を用いることで、生成物と反応物の濃度比からどちら側へシフトするかを予測可能です。
- 実験デザイン:新しい実験や研究計画を立てる際に、平衡定数があることで理論的根拠が得られます。
- 産業応用:化学工業などでは、生産効率やコスト削減につながるため、平衡定数の知識は極めて重要です。
また、平衡状態に達しているシステムでは、そのK値は一定であり、それによって系全体の挙動について深く理解できるようになります。例えば、生体内で行われる様々な生化学反応もこの原則に従います。私たちはその知識を活用し、新しい薬剤開発や環境問題への対処にも貢献しています。このように、平衡定数はただ単なる数字ではなく、多岐にわたる科学技術分野で必要不可欠な要素として機能します。
化学反応における平衡状態とは
、反応物と生成物の間で進行する過程が静的な状態に達したことを意味します。この時点では、反応は進行していないように見えますが、実際には分子レベルでは逆反応と正反応が同時に起こっており、その速度が等しくなることで全体の濃度は変化しません。私たちはこの現象を理解することで、平衡定数 何を意味するかという核心に迫ることができます。
平衡状態の特徴
平衡状態を理解するためには、以下の特徴を考慮する必要があります:
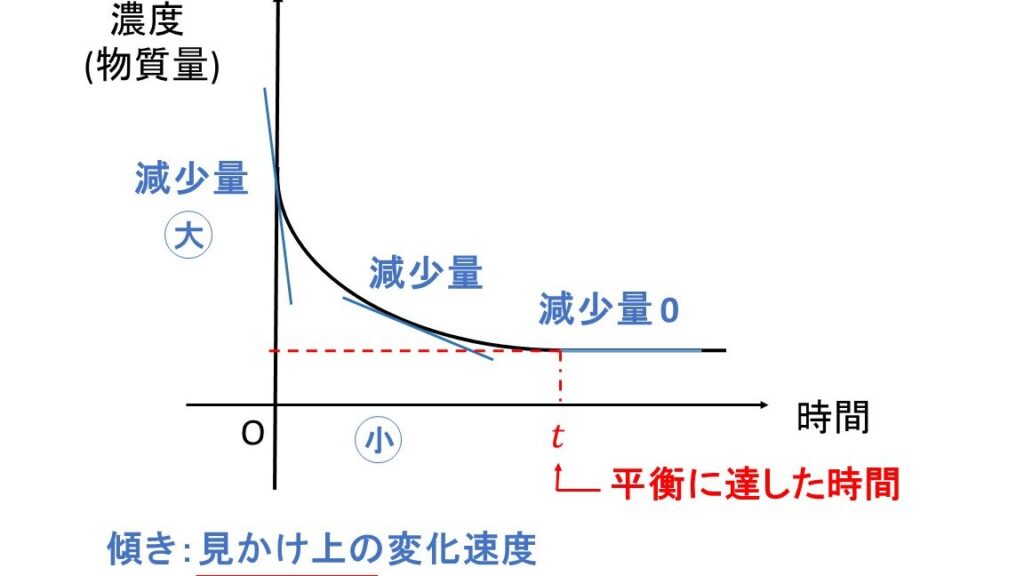
- 動的均衡:化学反応は常に進行していますが、正反応と逆反応の速度が等しいため、システム全体としては見かけ上変化しません。
- 温度依存性:平衡状態は温度によって影響されます。特定の温度下でのみ安定した平衡値となります。
- 外部条件への感受性:圧力や濃度などの外的要因も平衡状態に影響を与えることがあります。これらの変化によって、新たな平衡状態へ移行します。
平均濃度とK値
私たちが注目すべき重要な点は、この平衡状態で得られる平均濃度から計算される平衡定数(K値)です。K値は次式で表されます:
| 成分 | 濃度 |
|---|---|
| [生成物] | K = [生成物] / [反応物] |
このK値によって、それぞれの条件下でどれだけ生成物または反応物が存在すると予測できるかを示し、実際のプロセスへの適用可能性を探る手助けになります。
私たちはこの理論から得られる知識を活用し、多くの産業や研究分野で新しい発見や改良につなげています。その結果として、生体内でも多岐にわたる生理的機能や代謝経路なども、この平衡概念によって説明されています。
平衡定数の計算方法とその実例
平衡定数の計算は、化学反応における反応物と生成物の濃度を用いて行われます。私たちが前述したように、平衡状態では逆反応と正反応が同時に進行しているため、特定の条件下で各成分の濃度を測定することが重要です。このセクションでは、具体的な計算方法と実際の例を通じて、その理解を深めていきます。
平衡定数K値の計算式
平衡定数は以下の一般的な式で表されます:
| 反応式 | K = [生成物] / [反応物] |
|---|---|
| A + B ⇌ C + D | K = ([C] × [D]) / ([A] × [B]) |
ここで、それぞれの成分[A], [B], [C], [D]は、その時点でのモル濃度を示しています。この式からも明らかなように、生成物の濃度積を反応物の濃度積で割った値としてK値が求まります。
実例:水素とヨウ素による平衡反応
具体的な例として、水素(H2)とヨウ素(I2)が結合してヨウ化水素(HI)を生成する以下の反応を考えます:
| 化学反応式 | K = [HI]^2 / ([H2] × [I2]) |
|---|---|
| H2(g) + I2(g) ⇌ 2HI(g) |
仮にある条件下で、[H2]=0.5 M, [I2]=0.5 M, および[HI]=1.0 Mの場合、このシステムにおける平衡定数Kは次のようになります:
| K値計算結果 | |
|---|---|
| K = (1.0)^2 / (0.5 * 0.5) | = 4.0 |
これによって、この特定の状況下で得られるK値は4.0となり、これはこの化学系内でどれだけ生成物が存在可能かという指標となります。この結果からもわかるように、平衡定数はその系について多くを語ってくれる重要なパラメータなのです。
この計算方法や実例を通じて、「平衡定数 何を意味する」の理解がさらに深まることでしょう。次節では温度変化がこの平衡定数に与える影響について探求します。
温度変化が平衡定数に与える影響
温度は化学反応における平衡定数に大きな影響を与える要因の一つです。私たちは、特定の温度で平衡状態が達成され、その際の反応物と生成物の濃度から平衡定数が計算されることを理解しています。しかし、温度が変化すると、反応速度や生成物と反応物の比率にも変動が生じ、この結果として平衡定数も変わります。このセクションでは、温度変化による影響について詳しく探求していきます。
エンドサーモリック反応とエクソサーモリック反応
化学反応は一般的に、エンドサーモリック(吸熱)またはエクソサーモリック(発熱)に分類されます。それぞれのタイプによって、温度上昇時の挙動が異なります。
- エンドサーモリック反応: このような反応では、温度が上昇すると平衡定数は増加します。これは、高温環境下で吸収した熱エネルギーが生成物側へ移行しやすくなるためです。
- エクソサーモリック反応: 逆に、この場合は高温になると平衡定数は減少します。発熱する過程で余分な熱が供給されることにより、逆方向への進行(すなわち原料への再結合)が促進されるからです。
このように、それぞれのタイプによって異なる挙動を示すため、実際の化学プロセスではどちらか一方だけでなく両方を考慮する必要があります。
温度変化による具体例
以下に、具体的な例として水素とヨウ素からヨウ化水素を生成する過程を見てみましょう。この場合、水素とヨウ素間の関係性について検討します。
| 条件 | K値 (25°C) | K値 (50°C) |
|---|---|---|
| H2(g) + I2(g) ⇌ 2HI(g) | K = 4.0 | K = 6.5 |
この表からも明らかなように、水素とヨウ素との間で形成されるヨウ化水素の場合、高い温度設定ではK値が増加しています。これは、この特定の反応が吸熱的性質を持っているためであり、高温環境下では生成物側へのシフトが促進されています。
私たちの日常生活でも、このような現象はよく見られます。例えば料理中や工業プロセスなど、多くの場合で適切な温度管理によって効率的な成果を得ています。このことからも「平衡定数 何を意味する」の理解には、「温度」というパラメータを外せない重要要因として考慮し続けたいと思います。